Esponjas marinhas são os animais mais primitivos da Terra, tendo supostamente surgido há entre 500 milhões e 1 bilhão de anos. Este longo período de evolução possibilitou as esponjas marinhas a estabelecer associações estáveis e mutuamente benéficas com uma grande diversidade de micro-organismos. Estas associações são essenciais para a manutenção fisiológica e ecológica das esponjas, e também contribuem de maneira significativa para o sucesso ecológico destes animais no ambiente em que se encontram.
Quando a química destes animais começou a ser sistematicamente investigada há cerca de 50 anos, se observou que a química dos metabólitos secundários isolados destes animais é extremamente particular. Esponjas marinhas acumulam classes únicas e exclusivas de metabólitos secundários: alcaloides alquilpiridínicos e alquilpiperidínicos, alcaloides bromopirrólicos, alcaloides guanidínicos e alcaloides derivados da dibromotirosina, além de uma enorme diversidade de terpenos, policetídeos, derivados do ácido shiquímico, e outros metabólitos diversos.
À medida em que informações foram acumuladas sobre a química de esponjas, se verificou que vários metabólitos destes animais foram também isolados de meios de cultivo de micro-organismos diversos, não necessariamente isolados de esponjas. O fato de se encontrar as mesmas substâncias, ou substâncias muito parecidas, em esponjas e meios de cultivo de micro-organismos, levou os cientistas a postularem que os metabólitos de esponjas são, na verdade, produzidos por micro-organismos associados.
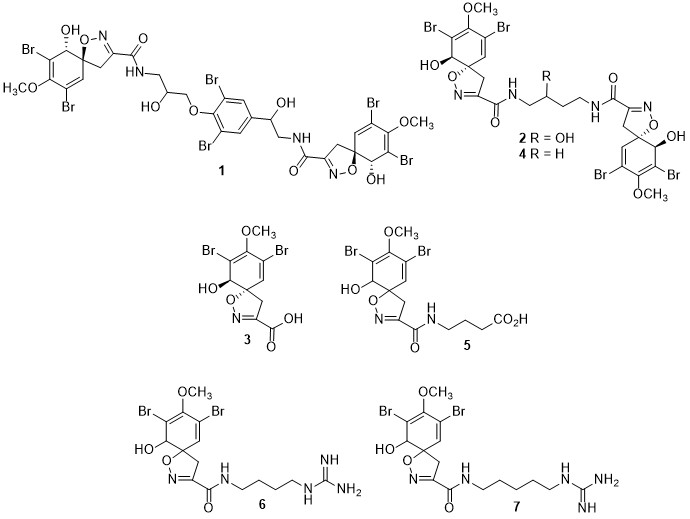
Neste trabalho, reportamos pela primeira vez o isolamento de derivados de dibromotirosina a partir do meio de cultivo de uma bactéria, Pseudovibrio denitrificans Ab134. Derivados de dibromotirosina são substâncias comumente isoladas de esponjas marinhas, principalmente da Ordem Verongida. A bactéria aqui estudada foi isolada a partir da esponja Arenosclera brasiliensis (Ordem Haplosclerida). A produção de dibromotirosinas por P. denitrificans Ab134 isolada de A. brasiliensis é extremamente surpreendente, e resolve o problema da origem destes metabólitos estruturalmente únicos. A importância deste trabalho é muito significativa para a comunidade de químicos de produtos naturais marinhos, microbiologistas marinhos, espongólogos e outros especialistas que se dedicam a investigar a química de associações simbióticas.
A realização deste trabalho só foi possível devido à dedicação de todos alunos envolvidos, em especial a Karen J. Nicácio. A excelente colaboração com os grupos dos Professores Fabiano Thompson (UFRJ), Eduardo Hajdu (UFRJ), Antonio G. Ferreira (UFSCar), Raymond J. Andersen (University of British Columbia), Alessandra Eustáquio (University of Illinois, Chicago), foi também de extrema importância. O sequenciamento do genoma de P. denitrificans Ab134 já foi realizado, objetivando investigar os genes que codificam a biossíntese dos derivados da dibromotirosina produzidos por esta bactéria. Leia nosso trabalho, aqui.
Curtir isso:
Curtir Carregando...



























Você precisa fazer login para comentar.